جداسازی DNA و RNA
جداسازی DNA و RNA توسط ژل آگارز الکتروفورز
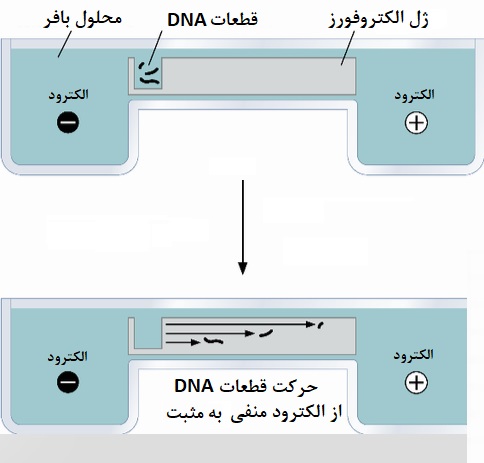
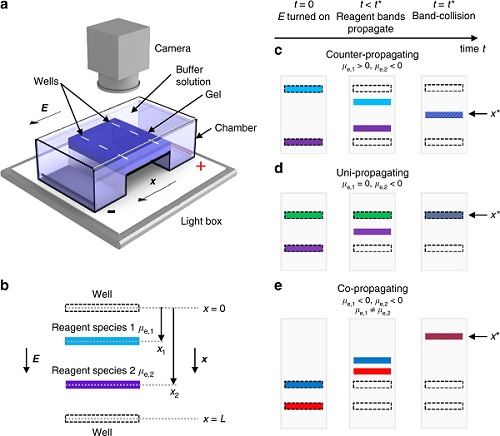
ژل آگارز روشی است که بطور معمول برای جداسازی پروتئین ها، DNA یا RNA مولکولهای اسید نوکلئیک به کمک اندازه از هم جدا می شوند، یک میدان الکتریکی که در آن مولکولهای با بار منفی به سمت آند حرکت می کنند (مثبت) و این ملکولها فقط بر اساس وزن مولکولی در داخل ژل حرکت میکنند به شکلی که مولکولهای با وزن کم سریع تر در داخل ژل حرکت میکنند.
علاوه بر اندازه جداسازی، تقسیم اسید نوکلئیک با استفاده از الکتروفورز ژل آگارز میتواند یک گام اولیه برای این امر باشد پس از خالص سازی نمونه مورد نظر “باند” از ژل رنگ آمیزی شده با استفاده از یک ترانسفیلومتر UV مشاهده میشود.
کاربرد الکتروفورز ژل آگارز در جداسازی DNA و RNA
الکتروفورز ژل آگارز دارای چندین مزیت است که سبب محبوبیت آن میشود. به عنوان مثال، اسیدهای نوکلئیک در طی فرایند جداسازی در ژل، اندازه شیمیایی آنها تغییر نمی کنند و ژل های آگارز را می توان به راحتی مشاهده و کنترل کرد. علاوه بر این، نمونه ها قابل بازیابی و برای مطالعات بیشتر از ژل ها به راحتی قابل استخراج می باشند. مزیت دیگر استفاده از الکتروفورز ژل آگارز این است که نتیجه ژل را می توان در یک کیسه پلاستیکی ذخیره کرد و پس از آزمایش در یخچال قرار داد تا برای مشاهده مجدد از آن استفاده کرد.
از الکتروفورز ژل آگارز به طور گسترده ای برای تخمین اندازه قطعات DNA استفاده می شود که بعد از هضم توسط آنزیم های محدود کننده قابل مشاهده است، نقشه برداری از محدوده DNA کلون شده در تشخیص ژنتیک مولکولی یا از طریق انگشت نگاری ژنتیکی، تجزیه و تحلیل محصولات PCR، جداسازی DNA ژنومی، جداسازی RNA قبل از Northern blot نیز مثال هایی هستند که به الکتروفورز ژل آگارز بستگی دارد.
نحوه مشاهده ژل آگارز
اتیدیم بروماید Ethidium bromide
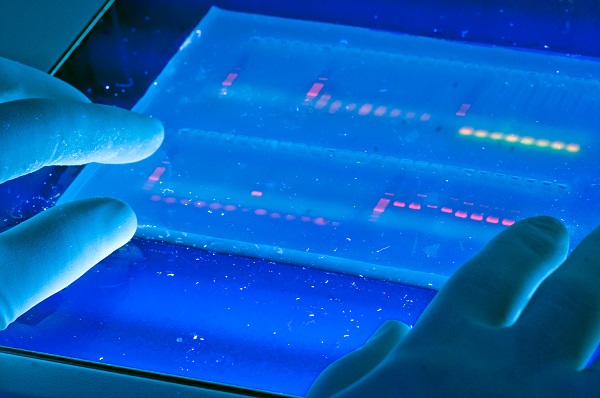
اتیدیم بروماید (EtBr) رنگ رایج جهت مشاهده اسید نوکلئیک است. روش های نوین نحوه استفاده از اتیدیم بروماید را توصیف می کند. (۲،۷-diamino-۱۰-etyl-۹-phenylphenanthridiniumbromide-) برای رنگ آمیزی DNA و RNA در ژل های آگارز مورد استفاده قرار می گیرد. از EtBr نیز برای رنگ آمیزی DNA یا RNA تک رشته ای استفاده می شود.
تحت اشعه ماوراء بنفش، حداکثر تحریک و انتشار فلورسانس از EtBr را می توان به دست آورد که از ۵۰۰- ۵۹۰ نانومتر است. قرار گرفتن DNA در معرض فلورسانس UV باید به سرعت انجام شود زیرا اسیدهای نوکلئیک در اثر قرار گرفتن در معرض طولانی تخریب می شوند، بنابراین وضوح باند کاهش یافته و تأثیر منفی خواهد بود.
.
.
مشاهده باندهای DNA
جهت مشاهده باندهای DNA از یک جایگزین به نام SYBR Green I که توسط Invitrogen تولید می شود می توان استفاده کرد. با وجود این واقعیت که SYBR گرین گران تر است، و ۲۵ برابر حساس تر از اتیدیم بروماید است. SYBR Safe، نوعی از SYBR Green است که نشان داده شده است که از سطح شفاف سازی کمی برخوردار است به علاوه SYBR Green جهش زایی و سمیت بسیار کم تری در مقایسه با اتیدیم بروماید دارد و این موضوع دلیل محکمی بر علاقه مندی محققین در استفاده از این ماده میباشد.
رنگ آمیزی و مشاهده DNA
از آنجا که DNA رنگ آمیزی شده EtBr در نور طبیعی قابل مشاهده نیست، بافرهای بارگذاری شده با بار منفی هستند که معمولاً قبل از بارگیری به ژل، به DNA اضافه می شود که برای بارگیری بافرها بسیار مفید هستند زیرا در نور طبیعی قابل مشاهده هستند و با DNA رسوب می کنند. زایلن cyanol و Bromophenol blue دو رنگ رایج است که به عنوان بافر بارگیری از آنها استفاده می شود.
اگر برخی از باندهای پس از جداسازی اندازه در ژل آگارز برای خالص سازی در نظر گرفته شده اند، تجزیه و تحلیل های بیشتر، توصیه میشود و از قرار دادن ژل در معرض نور UV خودداری کنید. به عنوان جایگزین، می توان از یک منبع تحریک نور آبی استفاده کرد.
.
مشکلات ایجاد شده در فرآیند الکتروفورز و جداسازی DNA و RNA
مشکل: اسمیر شدن باندها ممکن است به دلایل زیر رخ دهد:
۱- تجزیه شدن DNA توسط نوکلئازها
۲-شرایط نا مناسب الکتروفورز
۳- اثر GEL SHIFT
۴- بارگزاری بیش از اندازه DNA
۵- غلظت بالای نمک در نمونه
۶- شکلگیری نامناسب چاهک های ژل
مشکل: باقی ماندن DNA در چاهک
دلایل احتمالی:
۱-شکل گیری نا مناسب چاهک های ژل
۲-بارگیری بیش از اندازه DNA
۳-آلوده شدن نمونه DNA
۴- اثر GEL SHIFT
مشکل: باندهای منحنی شکل DNA
دلایل احتمالی:
۱-ژل به طور کامل در بافر الکتروفورز قرار نگرفته است.
۲-حجم نمونه ها کم می باشد.
۳-شرایط عمل الکتروفورز نامناسب است.
۴-حباب ها و یا ذرات بزرگی در چاهک های ژل و یا خود ژل موجود می باشند.